Zulassung ohne Wirksamkeit? Moderna`s neuer mRNA-Kombiimpfstoff
Die Europäische Kommission hat den ersten mRNA-Doppelimpfstoff von Moderna zugelassen. Die klinische Wirksamkeit wurde bisher jedoch nicht nachgewiesen.
Am 21. April 2026 gab der Pharmahersteller Moderna bekannt, dass er den mRNA-Kombinationsimpfstoff «mCOMBRIAX» gegen Influenza und SARS-CoV-2 in Europa auf den Markt bringen wird. Die Europäische Kommission hat diesen Impfstoff auf Empfehlung der Europäischen Arzneimittelagentur (EMA) zugelassen. Die EMA, die diese Empfehlung Ende Februar 2026 ausgesprochen hat, wird wiederum zu mehr als 91 % von der Pharmaindustrie finanziert. Laut Hersteller ist dies der «weltweit erste Impfstoff gegen Grippe und Corona». Er dient der «aktiven Immunisierung» und der Vermeidung von Influenza- und Corona-Erkrankungen bei Menschen über 50 Jahren. Die Studienautoren sind bei Moderna angestellt und könnten gemäß dem Abschnitt über potenzielle Interessenkonflikte Aktien des Unternehmens halten.
Schauen wir uns also an, auf Grundlage welcher wissenschaftlichen Erkenntnisse über den Nutzen dieses Präparats die Empfehlung und anschließend die Zulassung erfolgten.
In einer randomisiert-kontrollierten Studie wurden von insgesamt 8.000 Teilnehmern etwa 4.000 Menschen mit dem neuen Moderna-Impfstoff geimpft. Die Wirksamkeit der neuen Doppelimpfung wurde mit der Wirksamkeit zweier Gruppen verglichen, die Influenza- und/oder Corona-Impfungen erhielten. Ein Vergleich mit ungeimpften Personen war somit nicht möglich. Kriterium für die Teilnahme an der Studie war unter anderem, die von den staatlichen Behörden empfohlenen Corona-Impfungen vollständig erhalten zu haben. Völlig ungeimpfte Personen konnten somit nicht an der Studie teilnehmen.
Fehlender Nachweis der Wirksamkeit
Spätestens seit der Corona-Pandemie ist die Gesellschaft sensibler für die Aussagekraft der verkündeten Wirksamkeit von mRNA-Produkten. Die seit Jahren propagierte Wirksamkeit der Corona-Impfstoffe entsprach jedenfalls nicht den Ergebnissen der klinischen Zulassungsstudien. Diese zeigten nämlich nicht, dass die neu entwickelten Präparate insgesamt Leben retten. Trotzdem wurden sie von der EU-Kommission zugelassen und ebenfalls von der EMA empfohlen.
Wie so oft bei Impfstoffen liegt der Fokus der Studie zur neuen Doppelimpfung nicht auf der sorgfältigen Analyse klinisch relevanter Ergebnisse wie Erkrankungen oder Todesfällen, sondern auf den Antikörperwerten bis zu 29 Tage nach Verabreichung des Präparats. Aufgrund dieser kurzen Zeitspanne sind demnach keine Aussagen über die Antikörperwerte mehr als einen Monat nach der Impfung möglich. Es handelt sich also um ein kleines Zeitfenster und einen sehr eingeschränkten Blickwinkel. Die sogenannten „primären Endpunkte”, also die wichtigsten Parameter der Studie, setzen sich aus mehreren Messungen von Antikörpern gegen Corona und Influenza zusammen.
Aufgrund des Fehlens klinisch relevanter Daten schreiben die Studienautoren auch, dass «die Wirksamkeit von mRNA-1083 (Anmerkung des Autors: des neuen Doppelimpfstoffs) noch nicht nachgewiesen ist und daher noch weiter untersucht werden muss». Ziel der Studie war es lediglich, die »Nichtunterlegenheit« des neuen Präparats im Vergleich zu den zwei Einzelimpfstoffen gegen Influenza und SARS-CoV-2 zu zeigen. Auch der Ausschuss für Humanarzneimittel der EMA spricht in seiner Empfehlung lediglich von «Antikörperspiegeln gegen Influenza und SARS-CoV-2, die statistisch gesehen denen der Einzelimpfstoffe nicht unterlegen sind».
Auf Nachfrage teilt der Immunologe Dr. Kay Klapproth bezüglich des Parameters der Nichtunterlegenheit Folgendes mit: «Bemerkenswert bei dieser Art von Studien ist außerdem: Je schlechter der ursprüngliche Kontroll-Impfstoff ist, desto leichter ist es natürlich, die Nichtunterlegenheit des neuen Kandidaten nachzuweisen. Das ist sehr praktisch für die Hersteller. Stellen Sie sich vor, es würde ausreichen, wenn ihr jeweils neuestes Produkt nur 30 Prozent schlechter wäre als der Vorgänger. Bei Impfstoffen reicht das aus!»
Die Autoren thematisieren auch das Problem fehlender Wirksamkeitsnachweise und weisen darauf hin, dass es sich bei den angegebenen Antikörpermessungen um «etablierte Schutzkorrelate für die Wirksamkeit von Influenza- bzw. Corona-Impfstoffen» handelt. Das bedeutet, dass die im Vergleich zu Einzelimpfstoffen nur geringfügig erhöhten Antikörperlevel auch einen besseren Schutz vor einer Erkrankung bieten sollen. Doch wie sicher ist diese Annahme?
Auf Nachfrage äußert sich Dr. Kay Klapproth auch zur Aussagekraft des neuen Impfstoffs hinsichtlich seiner Wirksamkeit.«Die Studie hat nicht überprüft, ob der neue, mRNA-basierte Kombinationsimpfstoff tatsächlich vor Infektion oder Erkrankung schützt. Dieses vereinfachte Verfahren ist leider heute üblich. Stattdessen wurden Antikörper gemessen, also Surrogatmarker, die mit immunologischen Reaktionen korrelieren können, aber keine verlässliche Aussage über den klinischen Schutz erlauben. Im Zusammenhang mit Antikörpern von einem ‚etablierten Schutzkorrelat‘ zu sprechen, ist deshalb bestenfalls ‚missverständlich‘ – ich würde sogar von Täuschung sprechen. […]
Im konkreten Fall des neuen Moderna-Impfstoffs basiert die Bewertung im Wesentlichen auf neutralisierenden Antikörpern nach einem sehr kurzen Zeitraum von etwa vier Wochen. Das ist ausreichend, um eine Immunantwort zu dokumentieren, aber es reicht überhaupt nicht aus, um Aussagen über Dauer, Qualität oder klinische Schutzwirkung zu treffen. Man misst also eine Immunantwort und behauptet einfach, es sei Schutz. Das ist aber nicht korrekt.»
Auf Nachfrage äußert sich der Immunologe Prof. Andreas Radbruch wie folgt dazu: «Der Nachweis von möglicherweise schützenden Antikörpern im Blut ist kein Korrelat für Schutz vor Infektion und Infektiosität. Allein schon deshalb, weil die Antikörper im Blut zwar vor schweren Krankheitsverläufen schützen mögen, für den Schutz vor Infektion aber auf den Schleimhäuten sein müssten. Dafür müssten sie zunächst aus dem Blut transportiert werden. Das ist kein Automatismus. Kurz gefasst: Den Schutz einer Impfung vor Infektionen sollte man also epidemiologisch erfassen, d. h. wie viel weniger Menschen sich anstecken und wie viel weniger Menschen schwer erkranken.»
Von einer klinischen Wirksamkeit bezüglich der Verhinderung schwerer Atemwegserkrankungen ist in der Studie nichts zu lesen. Auch die sekundären Endpunkte beziehen sich ausschließlich auf Antikörperwerte.
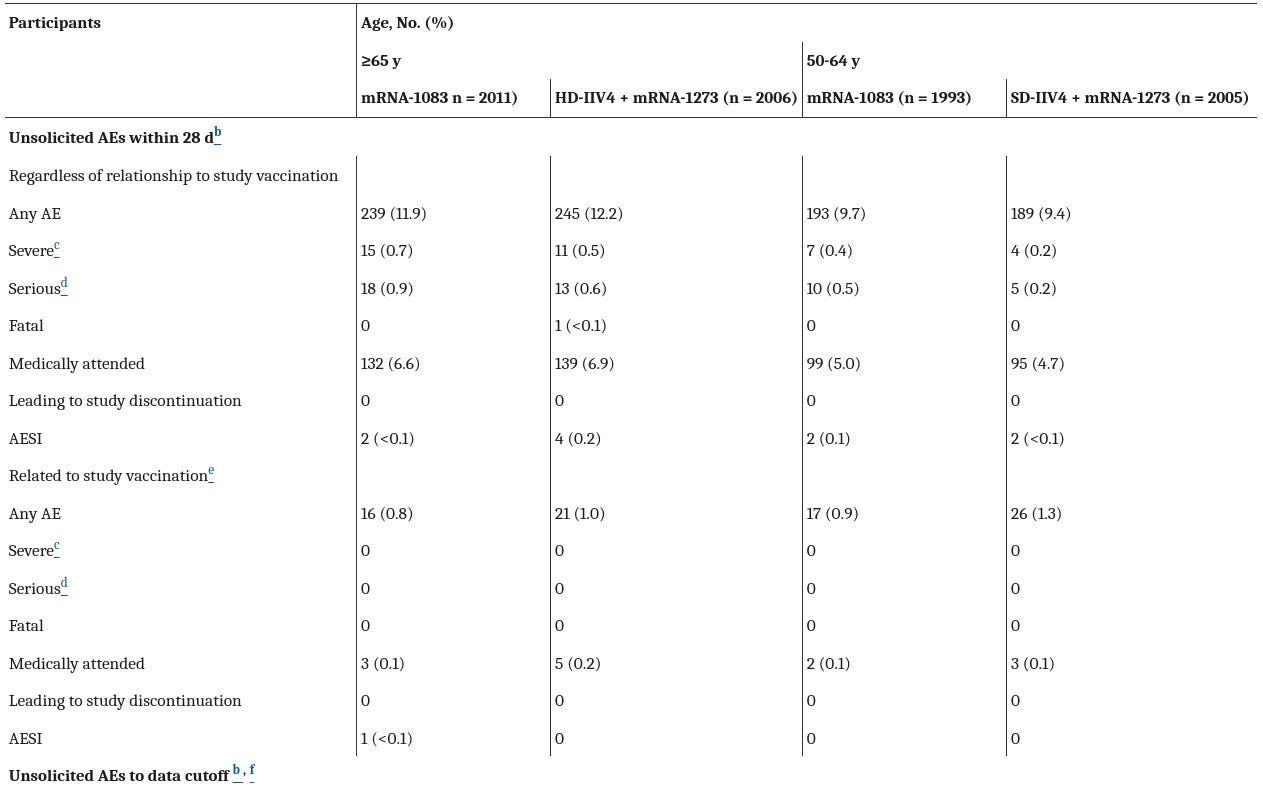
Die Studie erfasst auch die Anzahl der Nebenwirkungen und schwerwiegenden Nebenwirkungen in den verschiedenen Gruppen. Der Nachbeobachtungszeitraum für Nebenwirkungen beträgt bis zu 29 Tage, für schwerwiegende Nebenwirkungen bis zu sechs Monate. Das neue Moderna-Produkt ist den beiden Einzelimpfstoffen hinsichtlich der Nebenwirkungsrate nicht überlegen. Ein Vergleich mit einer Kontrollgruppe, die keine Impfung erhalten hat, ist aufgrund des Studiendesigns nicht möglich. Dennoch wären die Werte einer ungeimpften Vergleichsgruppe sehr interessant gewesen. Die Autoren stellen fest: «Es wurden keine schweren oder schwerwiegenden unerwünschten Ereignisse oder unerwünschten Ereignisse von besonderem Interesse als impfungsbedingt eingestuft, und es wurden keine Todesfälle oder Fälle von Myokarditis oder Perikarditis gemeldet.»
Ein Blick auf die Tabelle, die zur Studie gehört und unerwünschte Nebenwirkungen auflistet, bestätigt diese Aussage. Zu sehen sind die beiden Altersgruppen der Studie, jeweils mit dem neuen Kombiimpfstoff auf der linken Seite. Aufgelistet sind sogenannte AEs (Adverse Events) verschiedener Schweregrade. Das sind unerwünschte Arzneimittelwirkungen.
Die Abkürzung AESI steht für «Adverse Event of Special Interest» (unerwünschte Arzneimittelwirkungen von besonderem Interesse). Beide Impfstoffe haben ein ähnliches Nebenwirkungsprofil.
Fazit der Studienautoren
Nach der Abwägung von Nutzen und Risiken kommen die Studienautoren zu folgendem Schluss: «In dieser Studie erfüllte mRNA-1083 die Nichtunterlegenheitskriterien und löste stärkere Immunantworten aus als die empfohlene Standardbehandlung mit Influenza-Impfstoffen (Standard- und Hochdosis) sowie mit Impfstoffen gegen das Coronavirus. Dies geschah bei akzeptabler Verträglichkeit und einem akzeptablen Sicherheitsprofil.» Anstatt einen klaren Gesundheitsnutzen belegen zu können, sehen sich die Autoren gezwungen, von einem potenziellen Nutzen und Andeutungen zu sprechen. In der Studie heißt es: «Insgesamt deuten die Ergebnisse dieser Zwischenanalysen darauf hin, dass mRNA-1083 das Potenzial hat, mit einer einzigen Injektion Schutz vor zwei Atemwegserregern zu bieten und somit einen positiven Beitrag zur öffentlichen Gesundheit zu leisten.»
mRNA: Die Zukunft der Impfstoffhersteller
Die Autoren sehen jedoch neben der Nichtunterlegenheit noch andere Vorteile, die an den Beginn der Corona-Pandemie erinnern. Nur die im März 2020 nicht vorhandene, aber durch Medien, Politik und Politikberater vorgetäuschte Notlage ermöglichte die bedingte Zulassung der neuen mRNA-Technik für die Anwendung an gesunden Menschen. Diese verschaffte der Pharmaindustrie Milliarden, während das Risikoprofil für die geimpfte Bevölkerung bis heute eher unklar ist. Für die Berliner Zeitung schrieb ich diesbezüglich im September 2024:
«Ende November 2019 saß der Direktor der BARDA, Rick Bright, auf einem hochkarätigen Podium. Die Behörde der USA für „fortgeschrittene biomedizinische Forschung und Entwicklung“ (BARDA steht für Biomedical Advanced Research and Development Authority) ist eine Abteilung des Gesundheitsministeriums und war stark an der Erforschung und Produktion vieler Corona-Impfstoffe beteiligt.
Laut dem aktuellen Strategieplan von BARDA sollen derartige „Gegenmaßnahmen“ die Bevölkerung „vor Bedrohungen wie chemischen, biologischen, radiologischen und nuklearen Zwischenfällen schützen (unabhängig davon, ob diese versehentlich oder absichtlich herbeigeführt wurden)“. Der zivile Gesundheitsschutz wird so systematisch mit militärischen Fragen und Strategien verknüpft. Rick Bright machte auf besagtem Podium eine fast prophetisch wirkende Aussage. Er ging davon aus, dass der Ausbruch eines neuartigen Atemwegsvirus irgendwo in China nicht allzu abwegig sei.»
In der Studie wird auch die Bedeutung der mRNA-Plattform für diesen neuen Kombiimpfstoff erwähnt. Die Autoren schreiben dazu: «Darüber hinaus lässt sich die Plattform schnell anpassen, um zeitnah und wirksam im Bereich der öffentlichen Gesundheit zu handeln, insbesondere angesichts neu auftretender Varianten und Stämme.»
Auf der Startseite seiner Internetpräsenz wirbt der Pharmahersteller Moderna ganz prominent für die neuartige mRNA-Technologie. Dort heißt es: «Moderna hat sich zum Ziel gesetzt, mithilfe der mRNA-Technologie den größtmöglichen Mehrwert für Menschen zu erzielen. Dafür forschen wir an einer Vielzahl von mRNA-basierten Impfstoffen und Therapeutika.» Das Ziel besteht demnach eventuell darin, diesen Kombiimpfstoff als regelmäßige und anpassbare Impfung zu etablieren und damit die herkömmliche Grippeimpfung abzulösen.
Laut RKI-Daten hatte Letztere jedoch sogar eine «größtenteils negative Effektivität» in der Altersgruppe der über 60-Jährigen. Zu diesem Schluss kommt Karsten Montag in einem umfassenden Artikel über die Wirksamkeit von Schutzimpfungen gegen Corona und Influenza, der im Online-Magazin Multipolar erschienen ist.
Der Arzt und Sprecher des Vorstands des eingetragenen Vereins «Ärztinnen und Ärzte für individuelle Impfentscheidung» Dr. Alexander Konietzky formuliert folgende Einschätzung zur Zulassung des neuen Kombi-Impfstoffs: «Die zahlreichen Hinweise auf den begrenzten und risikobehafteten Einsatz der modRNA-Technologie scheinen für die Zulassungsbehörden keine Rolle zu spielen. Ganz zu schweigen von weiteren Schwachpunkten: keine Testung gegen Placebo, kein Nachweis einer klinischen Wirksamkeit, ausschließliche Bestimmung von Surrogatparametern, die nicht zur Feststellung des Nutzens geeignet sind. Mit dem neuen Grippe-COVID-19-Kombiimpfstoff sind wir auf dem fatalen Weg in die ‚Ein-Spritzen-Lösung‘.»
Es bleibt abzuwarten, wie viele Abnehmer es für diesen Impfstoff ohne nachgewiesene klinische Wirksamkeit in Europa geben wird. Seit der Corona-Impfkampagne und der damit verbundenen autoritären Politik sinkt das Vertrauen in Impfungen kontinuierlich. Insbesondere die Grippeschutzimpfung wird von älteren Menschen immer weniger akzeptiert. Die Tagesschau titelte Ende 2025: «In Deutschland haben sich zuletzt so wenig ältere Erwachsene gegen Grippe impfen lassen wie seit 17 Jahren nicht mehr. In der Saison 2024/2025 sank die Quote der Standardimpfung gegen Influenza bei Menschen ab 60 nach Angaben des Robert Koch-Instituts (RKI) auf 34 Prozent – das sind vier Prozentpunkte weniger als in der vorherigen Saison.»
Weitere Recherchen ermöglichen:
Bastian Barucker, GLS Bank, IBAN: DE02 4306 0967 1115 7847 01, BIC: GENODEM1GLS, Betreff: Schenkung
PayPal: info@bastian-barucker.de (Link)


Ein Satz in dem gut geschriebenen Aufsatz stimmt mich positiv. Die Akzeptanz dieser Möchtegern Impfstoffe nimmt kontinuierlich ab! Wenn das tatsächlich so sein sollte, ist das meiner Meinung nach das Einzige, was weiter hilft. Wenn der Profit wegbleibt, wird es schwierig für Big Pharma. Auch werden Regierungen sich nicht mehr so leichtfertig auf Knebelverträge einlassen. Trotzdem glaube ich, dass der Kampf erst begonnen hat!
Vor der Zulassung eines neuen Impfstoffes, müsste man halt zuerst einen Erreger nachweisen. Bis heute gibt es keine wissenschaftlichen Beweise für einen ansteckenden Virus. Im Gegenteil, mit Kontrollversuchen wurde die Ansteckungstheorie widerlegt!
Eine ungeimpfte Kontrollgruppe würde alles beweisen, aber welche
Fachzeitschrift dürfte das publizieren?